点蚀又称为孔蚀,是一种集中于金属表面很小的範围并深入到金属内部的腐蚀形态。点蚀一般是直径小而深度深。蚀孔的最大深度和金属平均腐蚀深度的比值,称为点蚀係数。点蚀係数愈大表示点蚀程度愈严重。
点蚀是一种破坏性和隐患较大的腐蚀形态之一,是化工生产及海洋事业中经常遇到的问题。
基本介绍
- 中文名:点蚀
- 外文名:pitting
- 类别:化学腐蚀
- 别名:孔蚀、小孔腐蚀
- 特点:腐蚀直径小而深度深
- 衡量标準:点蚀係数
基本概念
点蚀(又称孔蚀、小孔腐蚀等)是在金属上产生小孔的一种极为局部的腐蚀形态,而其地方几乎不腐蚀或腐蚀轻微。这类孔的直径有大有小,但在大多数情况下都比较小。
点蚀的特点
蚀孔由于孔径较小,洞口表面常有腐蚀产物遮盖。所以检查蚀孔时必须去除腐蚀产物否则是很难发现。
点蚀时的金属损失量很小,即使设备发生穿孔破坏,其设备的失重也很小,也难以用测量壁厚的减薄量来预测设备寿命。
点蚀由于它的特殊的动力学过程,反应是在自催化作用下加速进行的,点蚀一旦发生,孔内溶解速度相当大,所以点蚀的危害性很大,经常突然之间导致事故的发生,是破坏性和隐患较大的局部腐蚀形态之一。
蚀孔通常沿重力方向生长,设备中水平表面见得最多,少数发生在垂直表面,只有极少数在水平表面的底部上见到。
点蚀经常发生在具有自钝化性能的金属或合金上,并且在含氯离子的介质中更易发生如不鏽钢、铝和铝合金等在海水中发生的点蚀,碳钢在表而有氧化皮或层有孔隙的情况下,在含氯离子水中也会出现点蚀。
点蚀通常发生在静滞的溶液中,有流速或提高流速常可减轻或不发生点蚀。加大流速方面有助于溶解氧向金属表面的输送,使饨化膜容易形成和修复;另一方面可以减少沉积物及氯离子在金属表面的沉积和吸附,从而减少点蚀发生的机会,但当流速过高时,会对钝化膜起沖刚破坏作用,引起磨损腐蚀。介质温度升高,会使在低温下不发生点蚀的材料发生点蚀。
点蚀的机理
点蚀的发生到成核之前有一个很长的孕期,有的几个月或长达多年。点蚀在金属表面的伤痕、晶界、位错露头、金属内部的硫化物夹杂、晶界上的碳化物沉积等处优先形成,大多数情况下,在金属表面出现蚀孔后,蚀孔要继续发生长大。现以不鏽钢在充气含氯离子介质中的点蚀过程为例加以说明。
 图1
图1图1为不鏽钢在充气氯化钠溶液中点蚀过程的示意图。不鏽钢的点蚀起于纯化膜被氯离子所破坏而形成的点蚀源。蚀孔一旦形成,蚀孔内的表面就处于活性溶解状态,电位较负,成为阳极;蚀孔外的金属表面仍处于钝态,电位较正,成为阴极。于是蚀礼内外构成了一个活化-钝化的微电偶腐蚀电池:此电池具有大阴极、小阳极面积比的结构,所以阳极溶解速度很大,蚀孔问深处发展很快,而蚀孔金属钝化表面受到保护。
蚀孔内主要发生的阳极溶解反应有: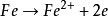 ,
, ,
,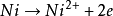 ,若介质呈中性或弱硷性时,蚀孔外钝化金属表面主要发生氧化极化反应:
,若介质呈中性或弱硷性时,蚀孔外钝化金属表面主要发生氧化极化反应: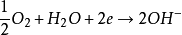 。由图可见,阴、阳极彼此分离,二次腐蚀产物在蚀孔口形成
。由图可见,阴、阳极彼此分离,二次腐蚀产物在蚀孔口形成 ,并进一步氧化成
,并进一步氧化成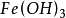 ,罩在蚀孔口,形成闭塞电池,导致蚀孔内介质相对于孔外介质呈流状态,溶解氧不易扩散进来,造成氧浓差电池。在蚀孔内溶解的金属离子不易向外扩,造成积累过多的正电荷,为维持孔内的电中性,有更多的氯离子迁人蚀孔内,形成氯化物、而氯化物将发生水解生成不溶性的金属氢氧化物和自由酸。因此,蚀孔底部的酸度增加,进一步加速了阳极的反应,这种由闭察电池引起的孔内酸化,从而加速金属腐蚀的作用,称为自催化作用。自催化过程的结果使蚀几不断向深处发展。
,罩在蚀孔口,形成闭塞电池,导致蚀孔内介质相对于孔外介质呈流状态,溶解氧不易扩散进来,造成氧浓差电池。在蚀孔内溶解的金属离子不易向外扩,造成积累过多的正电荷,为维持孔内的电中性,有更多的氯离子迁人蚀孔内,形成氯化物、而氯化物将发生水解生成不溶性的金属氢氧化物和自由酸。因此,蚀孔底部的酸度增加,进一步加速了阳极的反应,这种由闭察电池引起的孔内酸化,从而加速金属腐蚀的作用,称为自催化作用。自催化过程的结果使蚀几不断向深处发展。
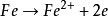

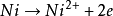
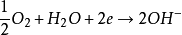

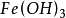
点蚀的防止
(1)从材料角度出发,可选用耐点蚀合金作为设备、部件的製造材料。不鏽钢中添加钼有助于不鏽钢的抗点蚀能力的增强,採用低碳、超低碳及硫化物杂质低的高纯不鏽钢,耐点蚀性能会得到显着改善。
在设备的製造、运输、安装过程中,保护好材料表面的光洁,不要划破或擦伤表而膜。注意焊渣等飞激物不要落在设备表面上,更不能在设备表面上引弧,对某些材料,增加壁厚可大大地延长蚀孔穿透时间。
(2)从环境、工艺角度出发,儘量降低介质中的氯离子、溴离子及氧化性金属离子的含量,能有效地防止点蚀。
(3)添加缓蚀剂,在循环水体系中,添加蚀剂可防止点蚀的发生,如对钝化型金属,添加缓蚀剂能增加钝化膜的稳定性和有利于受损的膜的修复。
(4)控制流速,不鏽钢等钝化型材料在滞流或缺氧的条件下易发生点蚀,控制适当的流速可防止点蚀。
(5)电化学保护,採用电化学方法也可抑制点蚀,通常为阴极保护。

